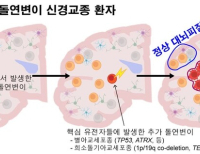
덴마크 제약사 노보노디스크제약(한국노보노디스크)의 GLP-1RA 계열 제2형 당뇨병 치료제인 ‘오젬픽프리필드펜’(Ozempic 피하주사제, 성분명 세마글루타이드, semaglutide)은 28일 식품의약품안전처로부터 만성신장병을 동반한 제2형 당뇨병 성인 환자에서 추정 사구체여과율(eGFR)의 지속적인 감소, 말기 신장병 도달 및 심혈관계질환 사망에 관한 위험 감소로 적응증 확대 승인을 받았다고 밝혔다.
국내 만 30세 이상의 당뇨병 환자에서 당뇨병성 신장질환 유병률은 약 4명 중 1명(25.4%)인 것으로 보고됐다. 당뇨병신장질환은 심혈관질환 이환율 및 사망률의 독립적인 위험인자로 작용하므로, 당뇨병과 합병증 관리는 필수적이다. 
이번 승인으로 오젬픽은 △제2형 당뇨병 조절이 충분하지 않은 성인에서 식이요법과 운동요법의 보조제로서 단독 투여 또는 다른 당뇨병 치료제와 병용 투여 △제2형 당뇨병과 확증된 심혈관계질환 성인 환자에서 주요 심혈관계 사건(MACE) 위험 감소 적응증에 이어 세 번째 적응증을 갖게 됐다. 이로써 국내 출시된 GLP-1RA 계열 제2형 당뇨병 치료제 중 폭넓은 범위의 적응증을 보유하게 됐다.
제2형 당뇨병이 있는 성인 환자에서 혈당 조절은 물론 주요심혈관계 사건(MACE) 위험 감소, 만성신장병을 동반한 제2형 당뇨병 성인 환자에서 추정 사구체여과율(eGFR)의 지속적인 감소, 말기 신장병 도달 및 심혈관계질환 사망 위험 감소까지 포괄하는 통합 치료 옵션으로서의 입지를 더욱 강화했다.
이번 오젬픽 만성신장병 적응증 확대는 ‘FLOW’ 3상 연구 결과를 근거로 이루어졌다. FLOW 연구는 다국가, 다의료기관, 위약 대조, 이중맹검, 피험자 1대1 무작위 배정 방식의 연구로, 만성신장병을 동반한 제2형 당뇨병 성인 환자 3533명을 대상으로 위약군 대비 오젬픽 투여군의 유효성 및 안전성을 평가했다.
이 연구의 1차 평가지표는 베이스라인(Baseline) 대비 지속적인 추정 사구체여과율(eGFR)의 50% 이상 감소 발생, 말기 신장병 발생, 심혈관계 또는 신장질환으로 인한 사망 등을 복합 평가한 변수로 설정됐다. 추적 관찰기간의 중앙값은 3.4년이었으며, 오젬픽 투여군은 위약군 대비 복합 평가변수 발생 위험을 24% 감소시킨 것으로 나타났다(HR, 0.76; 95% CI, 0.66-0.88; p=0.0003). 이 연구에서 보고된 중대한 이상반응은 오젬픽 투여군에서 877명(49.6%), 위약군에서 950명(53.8%)으로, 두 군 간에 유사한 것으로 나타났다.
캐스퍼 로세유 포울센 한국노보노디스크 대표는 “당뇨병 치료가 단순한 혈당 조절을 넘어, 심혈관 및 신장 위험까지 통합적으로 관리해야 하는시대에 진입했다”며 “노보노디스크는 100년 넘게 당뇨병 치료를 선도해 온 기업으로서 과학적 혁신과 축적된 경험을 통해 제2형 당뇨병 치료의 새로운 기준을 만들어가고 있다”고 밝혔다.