식품의약품안전처가 2025년 1월 한 달간 총 91개 의료제품을 허가했다. 허가 품목은 의약품 21개, 의약외품 2개, 의료기기 68개다. 이는 지난해 1월 허가 건수(122개)와 2024년 월평균(124개) 대비 각각 74.6%, 73.4% 수준으로 감소했다.
식품의약품안전처가 2025년 1월 한 달간 총 91개 의료제품을 허가했다. 허가 품목은 의약품 21개, 의약외품 2개, 의료기기 68개다. 이는 지난해 1월 허가 건수(122개)와 2024년 월평균(124개) 대비 각각 74.6%, 73.4% 수준으로 감소했다.
이번 허가 품목 중 주목할 만한 의약품은 희귀의약품으로 지정된 혈소판감소증 치료제 타발리스정(포스타마티닙나트륨수화물)과 중증 근무력증 치료제 비브가트주(에프가티지모드알파)다. 두 약물은 각각 제이더블유중외제약과 한독이 수입 허가를 받았다.
타발리스(Tavalisse) 2018년 4월 FDA 승인을 받은 품목으로 개발사는 리겔 파마슈티컬스다. 비브가트(Vyvgart)는 21년 12월 FDA 승인을 받았으며 원제약사는 아르젠엑스(argenx)로 모두 국내 제약사가 판권을 확보, 국내 허가됐다.
의료기기 분야에서는 인공지능(AI) 기반 소프트웨어 ‘JDA-01K’가 허가됐다. 이 제품은 환자의 임상 정보를 분석해 의사의 당뇨병 발병 위험도 결정을 보조하는 기능을 제공한다.
의약외품은 페리오민트향치약(엘지생활건강)과 파로돈탁스데일리후로라이드플러스치약(헤일리온코리아)이 허가됐다.
식약처는 앞으로도 안전하고 유효한 제품의 신속한 허가를 통해 환자 치료 기회를 확대할 계획이다. 또한 의료제품 허가 현황을 정기적으로 공개해 허가심사의 투명성과 신뢰성을 높일 방침이다.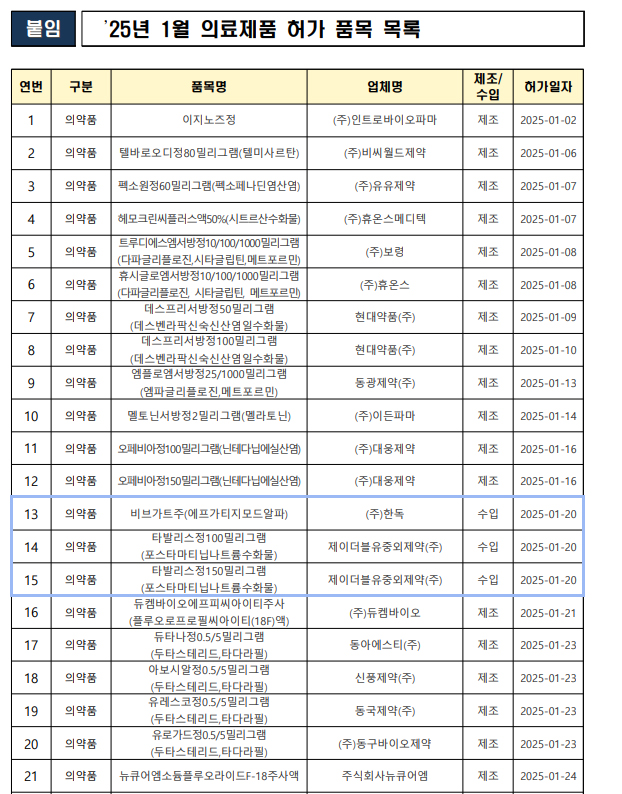 출처: 식약처, 의약품 허가현황
출처: 식약처, 의약품 허가현황